Tesamorelin-Tablettensind eine pharmazeutische Formulierung mit dem Wirkstoff Tesamorelin, die hauptsächlich zur Behandlung bestimmter Stoffwechselerkrankungen eingesetzt wird. Es handelt sich um ein künstlich synthetisiertes Analogon des Wachstumshormon-Releasing-Hormons (GHRH), das die Sekretion von Wachstumshormon (GH) aus dem Hypothalamus stimuliert und dadurch physiologische Prozesse wie den Fettstoffwechsel, die Proteinsynthese und das Knochenwachstum reguliert. Es kann direkt auf den GHRH-Rezeptor im Hypophysenvorderlappen einwirken und die Freisetzung von endogenem Wachstumshormon fördern, anstatt exogenes Wachstumshormon direkt zu ergänzen. Tesamorelin ist das einzige von der FDA zugelassene Medikament zur Behandlung der Bauchfettansammlung (Fettstoffwechselstörung) bei HIV-infizierten Personen. Bei HIV-Patienten kann es aufgrund einer langfristigen antiretroviralen Therapie (ART) zu einer Fettumverteilung (z. B. mehr Bauchfett und weniger Fett in den Gliedmaßen) kommen. Dieses Medikament kann das subkutane Fettvolumen im Bauch deutlich reduzieren und die Körperform verbessern.
Unsere Produkte



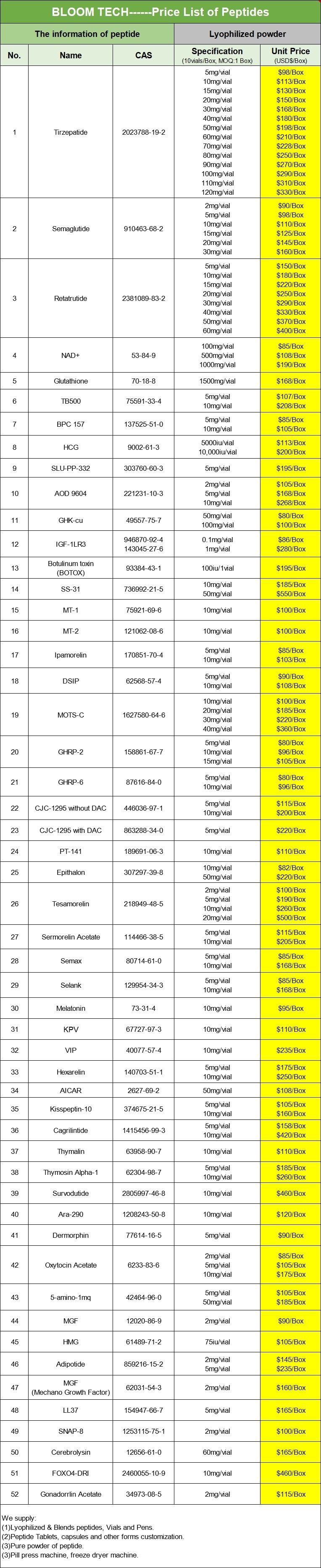
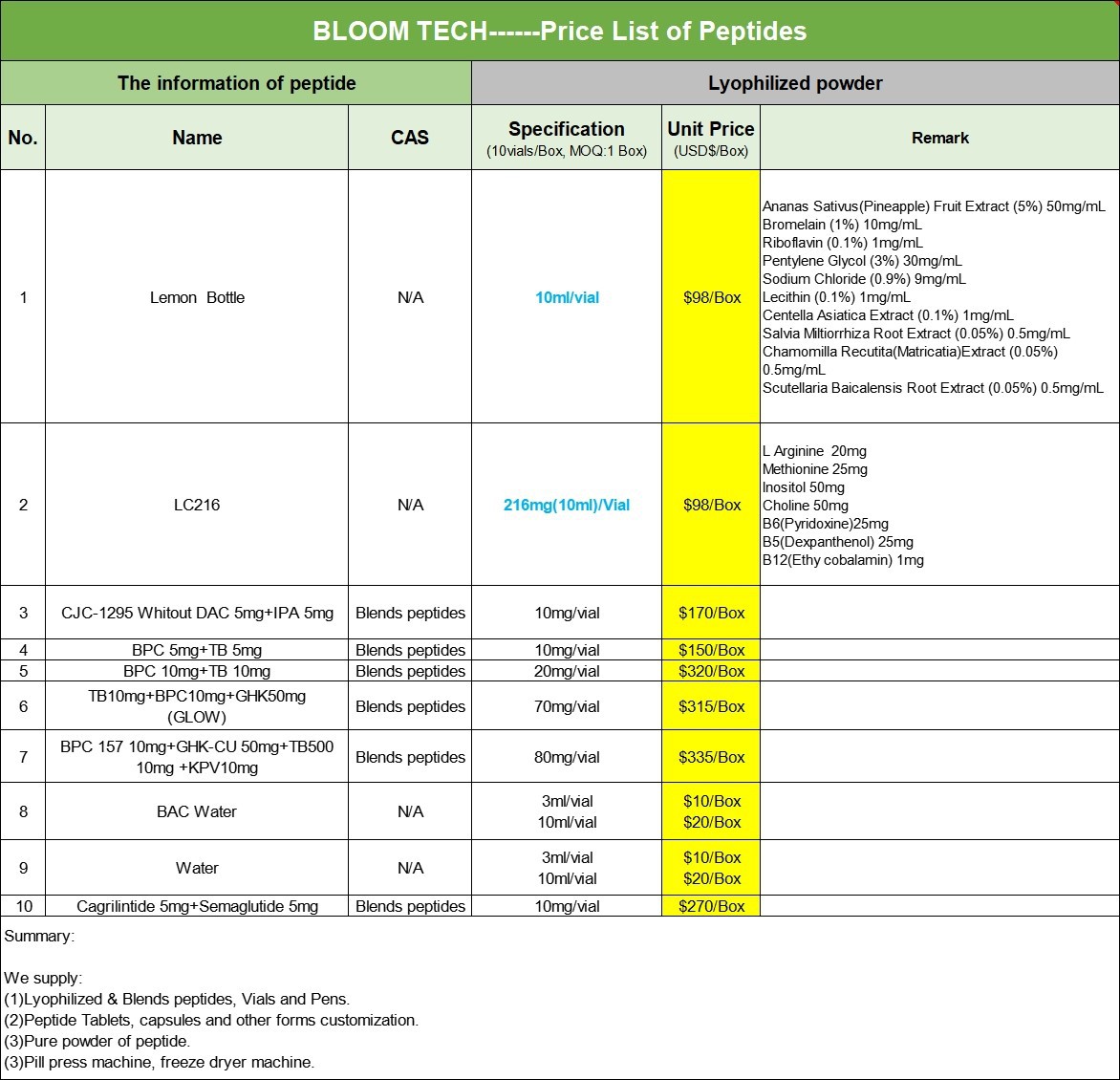

| Produktname | Tesamorelin-Pulver | Tesamorelin-Tabletten | Tesamorelin-Injektion |
| Produkttyp | Pulver | Tablette | flüssig |
| Produktreinheit | Größer oder gleich 99 % | Größer oder gleich 99 % | Größer oder gleich 99 % |
| Produktspezifikationen | 100g/1kg/usw. | 12,5 mg/20 mg | 2 mg/2 ml |
| Produktform | Organische Synthese | Oral einnehmen | Organische Synthese |
Tesamorelin COA
 |
||
| Analysezertifikat | ||
| Zusammengesetzter Name | Tesamorelin | |
| Grad | Pharmazeutische Qualität | |
| CAS-Nr. | 218949-48-5 | |
| Menge | 337,3 kg | |
| Verpackungsstandard | 25 kg/Trommel | |
| Hersteller | Shaanxi BLOOM TECH Co., Ltd | |
| Lot-Nr. | 202501090033 | |
| MFG | 9. Januar 2025 | |
| EXP | 8. Januar 2028 | |
| Artikel | Unternehmensstandard | Analyseergebnis |
| Aussehen | Weißes oder fast weißes Pulver | Konformiert |
| Wassergehalt | Weniger als oder gleich 5,0 % | 0.39% |
| Verlust beim Trocknen | Weniger als oder gleich 1,0 % | 0.28% |
| Schwermetalle | Pb Weniger als oder gleich 0,5 ppm | N.D. |
| Als weniger als oder gleich 0,5 ppm | N.D. | |
| Hg Weniger als oder gleich 0,5 ppm | N.D. | |
| Cd Weniger als oder gleich 0,5 ppm | N.D. | |
| Reinheit (HPLC) | Größer oder gleich 99,0 % | 99.80% |
| Einzelne Verunreinigung | <0.8% | 0.44% |
| Gesamtkeimzahl | Weniger als oder gleich 750 KBE/g | 80 |
| E. Coli | Weniger als oder gleich 2 MPN/g | N.D. |
| Salmonellen | N.D. | N.D. |
| Ethanol (durch GC) | Weniger als oder gleich 5000 ppm | 500 ppm |
| Lagerung | An einem verschlossenen, dunklen und trockenen Ort bei unter 2–8 Grad lagern | |
|
|
||

Tesamorelin-Tablettenist ein künstlich synthetisiertes Wachstumshormon-Releasing-Hormon (GHRH)-Analogon, das hauptsächlich zur Behandlung von Bauchfettstoffwechselstörungen eingesetzt wird, die durch eine antiretrovirale Therapie (ART) bei HIV-infizierten Personen verursacht werden.
Technische Herausforderungen und Lösungen für orale Tesamorelin-Tabletten
Abbau der Magensäure: Magensäure (pH 1,5–3,5) kann Amid- und Esterbindungen in Peptiden hydrolysieren, was zur Inaktivierung des Arzneimittels führt.
Enzymatische Hydrolyse im Darm: Trypsin, Chymotrypsin und andere Enzyme können Polypeptidketten gezielt spalten und so die Arzneimittelstruktur zerstören.
Feuchtigkeitsaufnahme: Tesamorelin neigt dazu, Umgebungsfeuchtigkeit zu absorbieren, was zur Verklumpung oder zum Abbau führt.
Stabilitätsprobleme und Schutzstrategien

Enteric coating technology: pH dependent polymers (such as hydroxypropyl methylcellulose phthalate, HPMCP) are used to coat the tablets, making them insoluble in the stomach and releasing the drug after entering the small intestine (pH>5.5).
Co-Abgabe von Enzyminhibitoren: Kombination von Darmenzyminhibitoren (wie Camostat, Soja-Trypsininhibitoren) oder Penetrationsverstärkern (wie Natriumcholat, Natriumlauroylsulfat), um den Arzneimittelabbau zu reduzieren und die Absorption zu fördern.
Stabilisierende Hilfsstoffe: Zugabe von Füllstoffen wie Mannitol und Laktose sowie Klebstoffen wie Hydroxypropylcellulose (HPC), um die Tablettenhärte und Feuchtigkeitsbeständigkeit zu verbessern.
Übermäßiges Molekulargewicht: Das Molekulargewicht von Tesamorelin (5111,6 Da) übersteigt bei weitem die Schwelle für den aktiven Transport durch Darmzellen (normalerweise).<500 Da), resulting in extremely low passive diffusion efficiency.
Polare Oberflächenladung: Die geladenen Gruppen von Peptiden (wie Arginin und Lysin) interagieren mit der Phospholipid-Doppelschicht der Zellmembran und behindern so den Transmembrantransport.
Penetrationsverbesserungstechnologie

Nanoträgertechnologie: Einkapselung von Arzneimitteln in Liposomen, Polymernanopartikeln oder festen Lipidnanopartikeln (SLNs), um die Absorption durch Endozytose oder Membranfusionsmechanismen zu fördern. Beispielsweise kann die Verwendung von Polymilchsäure-Hydroxyessigsäure-Copolymer (PLGA) zur Herstellung von Nanopartikeln die Verweildauer von Medikamenten im Darm deutlich verbessern.
Chemische Modifikation: Erhöhung der Lipophilie des Arzneimittels durch Modifikation von Polyethylenglykol (PEG) oder Fettsäurekonjugation. Zum Beispiel die kovalente Kombination von Tesamorelin mit Laurinsäure, um ein Prodrug zu bilden und die Membranpermeabilität zu verbessern.
Ionische Flüssigkeitstechnologie: Verwendung ionischer Flüssigkeiten (wie 1-Butyl-3-methylimidazoliumhexafluorphosphat) zum Auflösen von Arzneimitteln und zur Bildung niedrigviskoser Lösungen zur Verbesserung der Durchlässigkeit der Darmschleimhaut.
First-Pass-Effekt: Nachdem orale Medikamente über den Darm aufgenommen wurden, wird ein Teil davon von der Leber verstoffwechselt, was zu einer Verringerung der systemischen Exposition führt.
Individuelle Unterschiede: Es gibt individuelle Unterschiede im pH-Wert des Darms, der Enzymaktivität und der Expression von Transportproteinen, die sich auf die Konsistenz der Arzneimittelabsorption auswirken.

Optimierung der Bioverfügbarkeit

Mikronadelpflaster-unterstützte Verabreichung: In Kombination mit der transdermalen Mikronadeltechnologie werden Mikrokanäle auf der Oberfläche der Darmschleimhaut gebildet, um die direkte Wirkstoffabsorption zu fördern.
3D-Drucktechnologie: Maßgeschneiderte Tablettenstrukturen (z. B. mehrschichtige Tabletten, Kerne mit verzögerter Freisetzung), um eine gezielte Freisetzung von Arzneimitteln in bestimmten Teilen des Darms zu erreichen. Zum Beispiel mithilfe der FDM-Technologie (Fused Deposition Modeling) zum Drucken von Tabletten mit innerer Schicht, die Enzyminhibitoren enthalten, und Tabletten mit äußerer Schicht, die Medikamente enthalten.
Künstliche Intelligenz (KI) unterstütztes Design: Verwendung von Modellen des maschinellen Lernens zur Vorhersage von Arzneimittelhilfsstoffwechselwirkungen und Prozessparametern, Optimierung von Tablettenformulierungen. Verwenden Sie beispielsweise den Random-Forest-Algorithmus, um die optimale Dicke des Beschichtungsmaterials und die optimale Beladungskapazität für Nanopartikel zu ermitteln.
Herstellungsprozess von Tesamorelin-Tabletten zum Einnehmen

Vorbereitung der Rohstoffe
Solid phase synthesis: Using Wang resin as a carrier, amino acids are gradually coupled through Fmoc/tBu strategy to synthesize Tesamorelin linear peptide chains. Cut the resin with trifluoroacetic acid (TFA) to obtain crude peptides, and purify them by high performance liquid chromatography (HPLC) (purity>98%).
Gefriertrocknung: Die gereinigte Peptidlösung auf -80 Grad einfrieren, im Vakuum sublimieren, um Feuchtigkeit zu entfernen, und ein weißes, pulverförmiges Rohmaterial erhalten. Bei -20 Grad lagern, um Zersetzung zu vermeiden.
Aufbereitungstechnik

Magensaftresistent beschichtete Nanopartikeltabletten
Herstellung von Nanopartikeln: Es wurde die Methode der Emulgierungslösungsmittelverdampfung verwendet: Tesamorelin (5 % w/v) und PLGA (10 % w/v) wurden in Dichlormethan gelöst und mit einer Wasserphase gemischt, die Polyvinylalkohol (PVA, 2 % w/v) enthielt. Nach der Ultraschallemulgierung wurde das organische Lösungsmittel verdampft und die Nanopartikel durch Zentrifugation gesammelt.
Tablettenkomprimierung: Nanopartikel (30 % w/w), mikrokristalline Cellulose (50 % w/w) und Magnesiumstearat (2 % w/w) mischen und trocken komprimieren, um Kerntabletten zu erhalten. Überzug: Tauchen Sie die Kerntablette in eine Ethanollösung mit HPMCP (10 % w/v) und trocknen Sie sie, um eine magensaftresistente Überzugsschicht zu bilden.
Pellettabletten mit ionischer Flüssigkeit
Herstellung von Mikrokügelchen: Extrusionswalzverfahren: Tesamorelin (5 % w/v) in ionischer Flüssigkeit 1-Butyl-3-methylimidazoliumhexafluorphosphat auflösen, mit Hydroxypropylmethylcellulose (20 % w/v) mischen, in Streifen extrudieren und zu Mikrokügelchen (Durchmesser 1–2 mm) rollen.
Tablettenzusammenstellung: Mikrokügelchen (40 % w/w), Laktose (40 % w/w) und vernetztes Carboxymethylcellulose-Natrium (10 % w/w) mischen, nass granulieren, Tabletten pressen und überziehen.

Prozessvalidierung und -optimierung
Auflösungstest
Zur Bestimmung der Arzneimittelfreisetzungskurve unter Bedingungen von pH 1,2 (Magenflüssigkeitssimulation) und pH 6,8 (Darmflüssigkeitssimulation) wurde die USP-Typ-II-Paddelmethode verwendet, um die Integrität der magensaftresistenten Beschichtung sicherzustellen.
Stabilitätsstudie
Überprüfen Sie bei beschleunigten Tests (40 Grad / 75 % relative Luftfeuchtigkeit) und Langzeittests (25 Grad / 60 % relative Luftfeuchtigkeit) regelmäßig das Aussehen, den Inhalt und die zugehörigen Substanzen der Tabletten, um das Verfallsdatum zu bestätigen (normalerweise größer oder gleich 24 Monate).
Bioäquivalenztest (BE).
Durch eine Kreuzstudie mit gesunden Freiwilligen werden die Blutkonzentrations-Zeitkurven von oralen Tabletten und Injektionen verglichen, um zu überprüfen, ob die Bioverfügbarkeit dem Standard entspricht (normalerweise ist eine relative Bioverfügbarkeit von größer oder gleich 80 % erforderlich).
Die einzigartige Positionierung von Tesamorelin: Anders als die zielgerichtete Wirkung gewöhnlicher Wachstumshormon-Releasing-Peptide (GHRH)
Wachstumshormon freisetzendes Peptid (GHRH) ist ein vom Hypothalamus abgesondertes Neuropeptid, das den Stoffwechsel, das Wachstum und die Immunfunktion reguliert, indem es die Sekretion von Wachstumshormon (GH) im Hypophysenvorderlappen aktiviert. Herkömmliche GHRH-Analoga wie Sermorelin haben aufgrund ihrer kurzen Halbwertszeit und geringen Bioverfügbarkeit nur begrenzte klinische Anwendungen.Tesamorelin-Tabletten, als künstlich synthetisiertes GHRH-Analogon, haben durch strukturelle Optimierung und gezieltes Design signifikante Unterschiede in ihrem Wirkmechanismus, ihrer Pharmakokinetik und ihren klinischen Indikationen gezeigt, insbesondere bei der Behandlung von HIV-bedingten Lipidstoffwechselstörungen.
Molekulare Strukturunterschiede: von natürlichen Peptiden bis hin zu hochselektiven Analoga
Natürliches GHRH besteht aus 44 Aminosäuren (GHRH (1-44)), wobei sich seine aktive Kernregion an den N-terminalen Aminosäuren 1-29 befindet, von denen 1-21 essentielle Sequenzen sind und 22–29 die Rezeptorbindungsaffinität erhöhen. GHRH aktiviert den G-Protein-gekoppelten Signalweg durch Bindung an die extrazelluläre Domäne des GHRH-Rezeptors (GHRH-R) im Hypophysenvorderlappen und fördert so die GH-Synthese und -Freisetzung. Natürliches GHRH wird jedoch leicht durch Dipeptidylpeptidase IV (DPP-IV) im Blut abgebaut und weist eine gewisse Affinität zu GHRH-R in Geweben außerhalb der Hypophyse wie Fett und Muskeln auf, was zu Off-Target-Effekten führt.
Tesamorelin erreicht eine gezielte Verbesserung durch die folgenden strukturellen Modifikationen:
N-terminale Acetylierungsmodifikation: Einführung einer Acetylgruppe am N--Terminus von Histidin (His), um die Spaltstelle von DPP-IV zu blockieren und die Halbwertszeit - auf 2–3 Stunden zu verlängern (natürliches GHRH dauert nur 5–10 Minuten).
D--Aminosäuresubstitution: Ersetzen Sie L-Tryptophan an Position 2 durch D-Tryptophan, um die stereoselektive Bindung mit GHRH-R zu verbessern und die Kreuzaktivierung anderer G-Protein-gekoppelter Rezeptoren (wie VIP-Rezeptoren) zu reduzieren.
C-terminale Verkürzung und Funktionalisierung: Beibehaltung der 1-29-Kernsequenz des natürlichen GHRH, aber Einführung nicht natürlicher Aminosäuren (wie Methyllysin) durch chemische Synthese, um die Interaktion mit der Rezeptor-Transmembrandomäne zu optimieren und die Effizienz der Signalübertragung zu verbessern.
| Merkmal | Natürliches GHRH (1-44) | Tesamorelin |
| Aminosäurezusammensetzung | 44 L-Aminosäuren | 29 Aminosäuren (einschließlich D-Tryptophan) |
| Halbwertszeit- | 5-10 Minuten | 2-3 Stunden |
| Rezeptorselektivität | Niedrig (leicht kreuzaktivierbare VIP-Rezeptoren) | Hoch (aktiviert nur GHRH-R) |
| Enzymstabilität | Wird durch DPP-IV leicht abgebaut | Beständig gegen enzymatische Hydrolyse |
Gezielte Unterschiede in der Rezeptorbindung und Signaltransduktion
Verteilung und Funktion von GHRH-Rezeptoren
GHRH-R gehört zur Familie der G-Protein-gekoppelten Rezeptoren (GPCR) und wird hauptsächlich in Wachstumshormonzellen der Hypophyse exprimiert, aber auch in geringen Mengen im Fettgewebe, im Skelettmuskel, in der Bauchspeicheldrüse und in Immunzellen. Herkömmliche GHRH-Analoga wie Sermorelin können aufgrund ihrer geringen Affinität gleichzeitig Rezeptoren außerhalb der Hypophyse aktivieren, was zu Nebenwirkungen wie Insulinresistenz oder Lipolyse führt.
Gezielter Bindungsmechanismus von Tesamorelin
Bindung mit hoher Affinität
Die Bindungsaffinität von Tesamorelin zu GHRH-R (Kd ≈ 0,2 nM) ist aufgrund der verstärkten hydrophoben Wechselwirkung zwischen seinem D-Tryptophan und der extrazellulären Schleife des Rezeptors deutlich höher als die von natürlichem GHRH (Kd ≈ 1,5 nM).
Molekulare Docking-Simulationen zeigten, dass das C-terminale --Methyllysin von Tesamorelin in die hydrophobe Tasche der Rezeptor-Transmembrandomäne eingefügt werden kann, wodurch die Rezeptorkonformation stabilisiert und die Aktivierung des G-Proteins gefördert wird.
Organisationsspezifische Aktivierung
Hypophysen-Prioritäts-Targeting: Die Konzentration von Tesamorelin in der Hypophyse ist 10-20-mal höher als im Plasma, was auf die hohe Permeabilität des Hypophysenkapillarbetts für großmolekulare Peptide und die deutlich höhere lokale GHRH-R-Expressionsdichte im Vergleich zu peripheren Geweben zurückzuführen ist.
Desensibilisierung des peripheren Gewebes: Die Langzeitanwendung von Tesamorelin führt nicht zu einer Hochregulierung der GHRH-R-Expression in Fett oder Muskeln, während natürliches GHRH aufgrund einer anhaltenden Stimulation zu einer Herunterregulierung des Rezeptors führen kann, was zu einer Arzneimittelresistenz führt.
Selektivität des Signalwegs
Tesamorelin-TablettenAktiviert hauptsächlich den G s-cAMP PKA-Weg, fördert die GH-Gentranskription und hat schwächere Aktivierungseffekte auf den G i- oder G q-Wegen (die den Fettabbau oder Entzündungsreaktionen vermitteln können).
Tierversuche haben gezeigt, dass die Behandlung mit Tesamorelin die Freisetzung freier Fettsäuren aus dem Fettgewebe von Ratten nicht erhöht, während gleiche Dosen von natürlichem GHRH den Plasmaspiegel an freien Fettsäuren deutlich erhöhen können.
Beliebte label: Tesamorelin-Tabletten, Lieferanten, Hersteller, Fabrik, Großhandel, Kauf, Preis, Bulk, zu verkaufen






