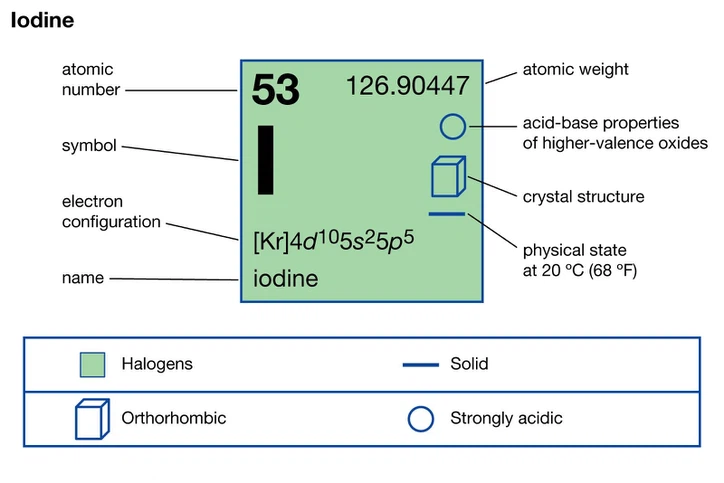
Die höhere Ionisationsenergie von Fluor im Vergleich zum Produkt ist ein faszinierendes Phänomen im Bereich der Chemie, insbesondere für Branchen wie Pharmazeutika und Spezialchemikalien. Dieser Unterschied in der Ionisationsenergie zwischen diesen beiden Halogenen beruht auf ihrer Atomstruktur und Position in der Periodenzüchter. Fluor, kleiner und weniger Elektronenschalen, benötigt mehr Energie, um ein Elektron aus seiner äußersten Hülle zu entfernen. Im Gegensatz,JodMit seiner größeren Atomgröße und mehr Elektronenschalen hat eine niedrigere Ionisationsenergie. Dieser grundlegende Unterschied in ihren elektronischen Eigenschaften spielt eine entscheidende Rolle bei ihrem chemischen Verhalten und ihren Anwendungen in verschiedenen Branchen.
Wir bieten Iodbälle CAS 12190-71-5. Weitere Informationen finden Sie auf der folgenden Website für detaillierte Spezifikationen und Produktinformationen.
Produkt:https://www.bloomtechz.com/chemical-reagent/laboratory-reagent/iodine-balls-caser-{4}.html
|
|
|
Atomstruktur und Elektronenkonfiguration: die Grundlage der Ionisationsenergie
Elektronenschalen -Theorie und ihre Auswirkungen auf die Ionisation
Die Atomstruktur von Elementen spielt eine grundlegende Rolle bei der Bestimmung ihrer Ionisationsenergie, die die Energie ist, die erforderlich ist, um ein Elektron aus einem Atom zu entfernen. Fluor mit einer Atomzahl von 9 hat eine relativ einfache Atomstruktur, wobei Elektronen nur in zwei Elektronenschalen angeordnet sind. Diese kompakte Anordnung bedeutet, dass sich die äußersten Elektronen in der Nähe des Kerns befinden, wo sie aufgrund der relativ geringen Größe des Atoms und des begrenzten Abschirmungseffekts durch innere Elektronen eine stärkere elektrostatische Anziehungskraft aufweisen. Infolgedessen braucht es mehr Energie, um diese starke Anziehungskraft zu überwinden und ein Elektron aus Fluor zu entfernen, was ihm eine höhere Ionisationsenergie verleiht. Im Gegensatz,JodMit einer Atomzahl von 53 hat eine viel komplexere Atomstruktur mit fünf Elektronenschalen. Die äußersten Elektronen in den Produkten befinden sich weiter vom Kern entfernt, wodurch die Stärke der Anziehung, die sie aus den positiv geladenen Protonen im Kern erleben, verringert. Darüber hinaus liefern die inneren Elektronenschalen in Jod zusätzliche Abschirmung und schwächen den Zug der äußeren Elektronen weiter. Dieser erhöhte Abstand und die Abschirmung haben es einfacher, ein Elektron aus Jod zu entfernen, was zu einer niedrigeren Ionisationsenergie im Vergleich zu Fluor führt. Daher wirkt sich der Unterschied in der Atomstruktur zwischen den beiden Elementen erheblich auf die für die Ionisierung erforderliche Energiemenge aus.
Nuklearladung und Abschirmungseffekte
Ein weiterer Schlüsselfaktor, der die Ionisationsenergie beeinflusst, ist die wirksame Kernladung der äußersten Elektronen. Im Falle von Fluor enthält sein Kern im Vergleich zu Jod weniger Protonen, übt jedoch eine konzentriertere Kernladung für seine Valenzelektronen aus. Dies liegt daran, dass Fluor weniger Elektronenschalen hat, was bedeutet, dass die äußeren Elektronen näher am Kern sind und sich stärker davon angezogen fühlen. Andererseits hat es einen größeren Kern mit mehr Protonen, aber auch mehrere innere Elektronenschalen, die einen Abschirmeffekt erzeugen. Diese inneren Elektronen blockieren oder reduzieren die attraktive Kraft zwischen den äußeren Elektronen und dem Kern, was es den äußeren Elektronen schwieriger macht, die volle Belastung der Kernladung zu spüren. Infolgedessen sind die äußeren Elektronen in den Produkten im Vergleich zu Fluor weniger eng an den Kern gebunden. Dieser Abschirmeffekt in Jod führt zu einer niedrigeren Ionisationsenergie, da weniger Energie erforderlich ist, um ein Elektron aus seiner äußersten Hülle zu entfernen. Die Kombination der größeren Größe von Iodin und dem Abschirmung erleichtert die Ionisierung im Vergleich zu Fluor, was aufgrund ihrer stärkeren Anziehungskraft zwischen den Nucleus- und Valenzelektronen eine höhere Ionisationsenergie aufweist.
Wie beeinflusst die Atomgröße die Ionisationsenergie zwischen Fluor und Jod?
Die inverse Beziehung zwischen Atomgröße und Ionisationsenergie
Die Atomgröße ist ein entscheidender Faktor für die Bestimmung der Ionisationsenergie eines Elements. Im Allgemeinen besteht eine inverse Beziehung zwischen Atomgröße und Ionisationsenergie: Wenn die Atomgröße zunimmt, nimmt die Ionisationsenergie tendenziell ab. Dieser Trend kann beim Vergleich von Fluor und Vergleich klar beobachtet werdenJod. Fluor mit einem kleineren Atomradius hat seine Elektronen vom Kern fester gehalten. Der kürzere Abstand zwischen dem Kern und den äußersten Elektronen führt zu einer stärkeren attraktiven Kraft, die mehr Energie erfordert, um diese Anziehung zu überwinden und ein Elektron zu entfernen. Aus diesem Grund hat Fluor eine relativ hohe Ionisationsenergie. Andererseits hat Jod einen viel größeren Atomradius, was bedeutet, dass seine äußeren Elektronen weiter vom Kern entfernt sind und durch zusätzliche innere Elektronenschalen abgeschirmt sind. Infolgedessen erleben die äußeren Elektronen im Produkt einen schwächeren Zug aus dem Kern, was es einfacher zu entfernen ist. Dies erklärt, warum es eine niedrigere Ionisationsenergie im Vergleich zu Fluor aufweist. Die größere Atomgröße des Produkts führt zu einer diffuseren Elektronenwolke, die die Energie reduziert, die erforderlich ist, um das Atom zu ionisieren. Daher spielt die Atomgröße eine grundlegende Rolle bei der Beeinflussung dessen, wie leicht ein Elektron aus einem Atom entfernt werden kann.
Elektronelektronenabstoßung und ihre Auswirkungen
Der Größenunterschied zwischen Fluor und Produkt beeinflusst auch die Elektronenelektronenabstoßung. Bei einem kleineren Atom von Fluor sind die Elektronen näher beieinander und erhöhen abstoßende Kräfte. Paradoxerweise senkt diese Abstoßung die Ionisationsenergie nicht, da die Kernattraktion dominiert. In Iods größerem Atom verringert der erhöhte Abstand zwischen Elektronen die Abstoßung, schwächt aber auch den nuklearen Zug der äußeren Elektronen, was letztendlich zu einer niedrigeren Ionisationsenergie führt.
|
|
|
Praktische Implikationen der Ionisationsenergieunterschiede in der chemischen Industrie
Anwendungen in der pharmazeutischen und speziellen chemischen Synthese
Der Unterschied in der Ionisationsenergien zwischen Fluor undJodhat tiefgreifende Auswirkungen auf die Pharma- und Spezialchemieindustrie. Fluor mit seiner hohen Ionisationsenergie ist eine ausgezeichnete Elektronen-With-Drawing-Gruppe in Arzneimittelmolekülen. Diese Eigenschaft verbessert die Stoffwechselstabilität von Arzneimitteln und macht sie resistenter gegen den Zusammenbruch des Körpers und verbessert damit ihre Wirksamkeit. Andererseits dient Jod mit seiner niedrigeren Ionisationsenergie als gut verlassene Gruppe in der organischen Synthese. Dies macht Jod zu einer wertvollen Komponente bei der Erleichterung chemischer Transformationen, die für die Entwicklung neuer pharmazeutischer Verbindungen und Spezialchemikalien wesentlich sind. Die kontrastierenden Eigenschaften von Fluor und Jod spielen Schlüsselrollen bei der Optimierung des Arzneimitteldesigns und der chemischen Synthese.
Auswirkungen auf industrielle Prozesse und materielle Eigenschaften
In industriellen Anwendungen beeinflussen die Ionisation -Energie -Unterschiede die chemische Reaktivität und die Bildung von Bindungen. Die hohe Ionisationsenergie von Fluor trägt zu seiner starken Elektronegativität bei, wodurch es wertvoll ist, hochstabile Verbindungen zu erzeugen, die in Polymeren und Spezialmaterialien verwendet werden.JodinEine niedrigere Ionisationsenergie macht sie bei der Katalyse und als reaktives Intermediat in verschiedenen chemischen Prozessen nützlich, insbesondere bei der Synthese komplexer organischer Moleküle. Das Verständnis dieser grundlegenden Eigenschaften von Fluor und dem Produkt ist für Branchen, die sich mit chemischer Synthese und Materialentwicklung befassen, von entscheidender Bedeutung. Weitere Informationen darüber, wie diese Eigenschaften in Ihren spezifischen Anwendungen genutzt werden können, kontaktieren Sie uns bitte unter uns unterSales@bloomtechz.com.
Referenzen
1. Atkins, PW & de Paula, J. (2010). Atkins 'physikalische Chemie. Oxford University Press.
2. Hoosecroft, CE & Sharpe, AG (2012). Anorganische Chemie. Pearson Education Limited.
3. Cotton, FA, Wilkinson, G. & Gaus, PL (1995). Grundlegende anorganische Chemie. John Wiley & Sons.
4. Greenwood, NN, & Earnshaw, A. (1997). Chemie der Elemente. Butterworth-Heinemann.